实验室关于支持细胞功能和增殖调控的最新研究结果正式发表
2020-09-26
雄性动物的生殖力取决于睾丸生精小管中功能配子的生成。在哺乳动物中,支持细胞是唯一与发育中的生精细胞直接相互作用的体细胞。支持细胞为生精细胞提供结构和功能上的支持以保障精子发育。利用细胞去除等实验,不同实验室提供的数据表明支持细胞数量直接决定了睾丸的大小和每日精子的产生,支持细胞也影响睾丸的血管结构和睾丸激素的分泌。从细胞调控的角度看,支持细胞是一类独特的细胞,仅在胎儿期和青春期之前增殖,在成年性腺中维持在静止状态。揭示支持细胞发育过程和功能的分子机制对于了解动物正常精子发生和生殖缺陷至关重要,但目前,支持细胞是否以及如何调控性原细胞发育并不清楚,我们对支持细胞增殖和成熟调控机制的了解也十分有限。
高原动物生殖生物学科组利用Amh-Cre介导在胚胎期生殖细胞中产生白喉毒素以减少支持细胞数量,发现在胚胎期14.5天支持细胞数量显著降低。在正常小鼠中,性原细胞有丝分裂阻滞于胚胎期16.5天,而支持细胞丢失小鼠中性原细胞在胚胎期16.5天依然处于增殖状态并表达减数分裂标记蛋白gH2AX与SYCP3,表明支持细胞抑制胚胎期性原细胞进入减数分裂过程。出生后,支持细胞损失也对性原细胞重新进入细胞周期发挥作用。另外我们利用支持细胞特异表达GFP的转基因小鼠分离纯化支持细胞,并对胚胎期12.5天、13.5天、16.5天和出生后1天的支持细胞进行转录组动态分析,揭示了独特的基因表达模式和调控支持细胞发育和生殖细胞与支持细胞相互作用的潜在候选基因。
另外,我们发现转录因子E4F1作为一种调控细胞增殖、代谢和干细胞命运决定的多功能蛋白,在睾丸中主要富集于早期支持细胞和精原细胞和成年后支持细胞中。我们构建了E4f1支持细胞特异性敲除小鼠模型,以研究E4F1在支持细胞中的功能。结果表明E4F1缺失导致睾丸大小和生育能力降低,进一步的分析显示减数分裂进程和精子发生正常,但出生后支持细胞的增殖能力受到限制,支持细胞数量减少、生殖细胞凋亡增加。这些结果表明,转录因子在小鼠支持细胞中表达,并在调节支持细胞增殖和生殖力中起重要作用。
相关论文Function and transcriptomic dynamics of Sertoli cells during prospermatogonia development in mouse testis和E4 transcription factor 1 (E4F1) Regulates Sertoli cell Proliferation and fertility in mice分别于2020年9月17日和2020年9月18日在Reproductive Biology和Animals发表。博士研究生闫荣格为第一作者,杨其恩研究员为通讯作者。该研究得到了国家自然基金面上项目(31571539和31771656)、青海省自然科学基金(2020-ZJ-902)和青海省千人计划等项目的支持。
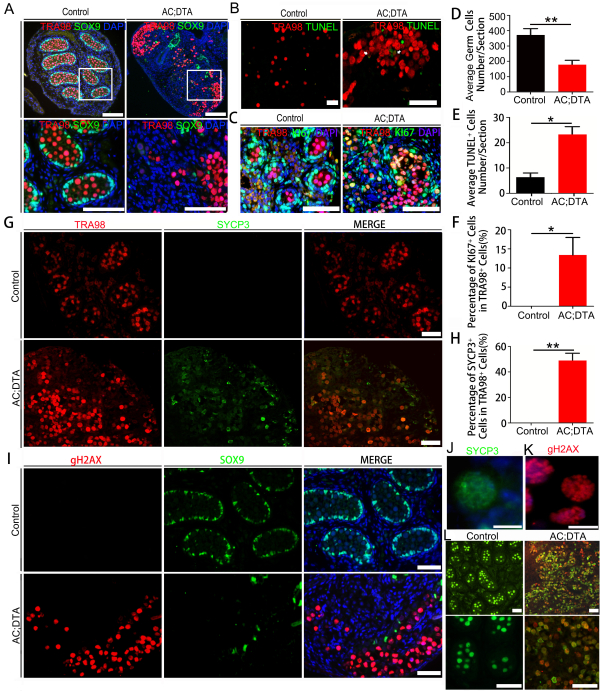
支持细胞丢失导致胚胎期16.5天性原细胞处于增殖和减数分裂状态(Yan et al, Reproductive Biology, 2020)
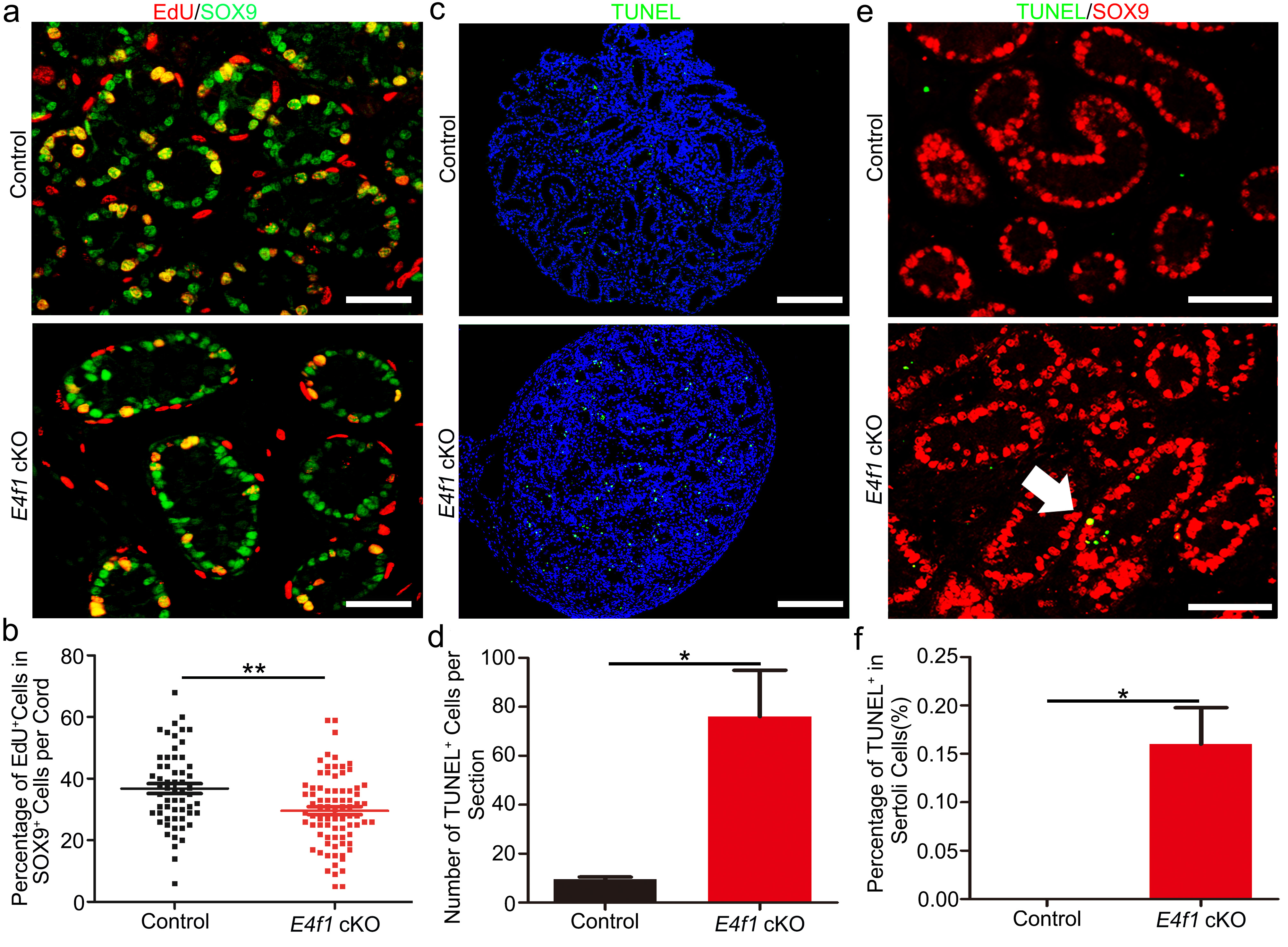
支持细胞特异性敲除E4f1导致小鼠亚不育,出生后支持细胞增殖损伤和凋亡增加 (Yan et al., Animals, 2020)